آشنایی کامل با باتری لیتیوم یونی به زبان ساده (راهنمای جامع و کامل باتری لیتیوم یونی)
به گزارش مجله کیف ابزار، همه ما با شروع یک روز جدید با لوازمی سر و کار داریم که به احتمال زیاد از باتریهای لیتیومی برای تامین انرژی موردنیاز خود استفاده میکنند. ساعت، مسواک برقی، لپتاپ، تبلت و از همه مهمتر گوشی تلفن همراه! حتی بسیاری از خودروهای جدید نیز به باتریهای لیتیومی یا لیتیوم-یونی مجهز هستند. به طور کلی فناوری باتریهای لیتیومی به عنوان منبع انرژی بسیاری از تجهیزات و ابزارهای برقی زندگی ما محسوب میشود و استفاده از این تکنولوژی در طراحی ابزارهای برقی به سرعت در حال افزایش است.
با اینکه باتریهای لیتیومی به دلیل برخورداری از سطح ایمنی بالا به انتخاب اول بسیاری از تولیدکنندگان تبدیل شدهاند اما سوال مهم اینجاست که باتری لیتیومی چیست؟ چه ساختاری دارد؟ و برای انجام چه کارهایی میتوان از آن استفاده کرد؟
باتریهای لیتیومی از چه موادی ساخته میشوند؟
فرآیند آزادسازی الکترون و تولید جریان الکتریکی در همه باتریها به وسیله انجام واکنشهای شیمیایی انجام میشود و جای تعجب نیست که نامگذاری باتریها بر اساس مواد و عناصر تشکیلدهنده آنها صورت میگیرد. به عنوان مثال بسیاری از باتریهای قلمی از نوع NiMH هستند یا برخی از ابزارهای شارژی قدیمی از باتریهای NiCD (نیکل-کادمیویم) استفاده میکنند.
عنصر لیتیوم نیز به عنوان ماده اصلی مورد استفاده در باتریهای لیتیوم-یونی است که ویژگیهای منحصربفردی را برای انجام واکنشهای شیمیایی و تولید جریان الکتریکی در اختیار ما قرار میدهد.
باتری های لیتیومی توسط چه کسی اختراع شد؟
بدون شک نمیتوانیم به سادگی از موضوع اختراع باتری های لیتیومی عبور کنیم اما باید بدانیم که پایهگذاری و تولید اولین نمونه از باتری های لیتیومی امروزی، بر پایه تلاشهای سه شخص مختلف صورت گرفته است. پیش از تولید باتریهای لیتیومی، شخصی به نام Michael Stanley Whittingham (مایکل استنلی ویتینگهام) برای اولین بار نظریه الکترودهای موازی را در دهه 1970 میلادی مطرح کرد که امروزه به عنوان پایه و اساس فرآیند شارژ و تخلیه باتریهای لیتیومی شناخته میشود.
آقای استنلی اولین نمونه از باتری های لیتیوم-یونی شارژی را با استفاده از کاتد دی سولفید تیتانیوم و آنُد آلومینیوم لیتیوم تولید کرد. (کاتد به معنی الکترود منفی و آند به معنی الکترود مثبت است.)
پس از استنلی، شخصی به نام John Goodenough (جان گودناف) در اوایل دهه 1980 با استفاده از اکسید لیتیوم کبالت در نقش کاتد، موفق به تولید نوع دیگری از باتریهای لیتیومی شد که از نظر ایمنی در درجه بالاتری قرار میگرفت.
در نهایت یک فرد ژاپنی به نام Akira Yoshino (آکیرا یوشینو) اولین نمونه از باتریهای لیتیومی امروزی را در سال 1985 معرفی کرد که به جای استفاده از لیتیوم دارای یک آند کربنی بود. همین موضوع باعث شد که شرکت سونی در سال 1991 از باتریهای لیتیومی به شکل گسترده در تولید تلفنهای همراه خود استفاده کند.
جریان الکتریسیته چگونه در یک سلول لیتیوم یونی به وجود میآید؟
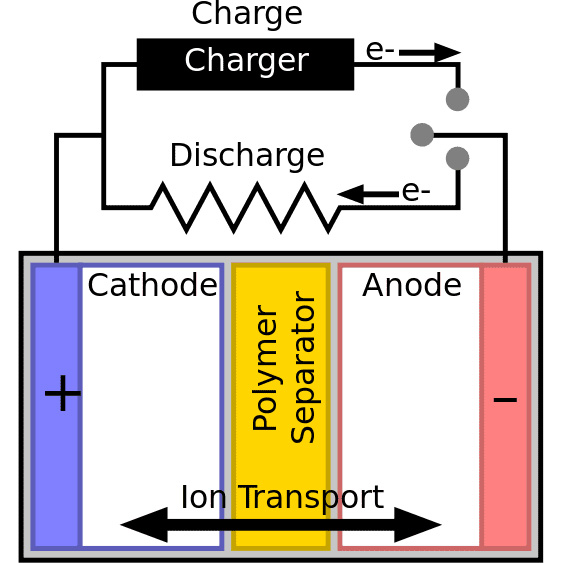
حضور دو الکترود فلزی (آند و کاتد) برای انجام واکنش شیمیایی در سلولهای باتری الزامی است که معمولا از آلومینیوم در بخش کاتد و از مس در بخش آند استفاده میشود اما رایجترین ترکیب در ساختار باتریهای لیتیومی شامل اکسید لیتیوم کبالت در بخش کاتد و گرافیت در بخش آند است و بیشتر باتریهای مورد استفاده در لپتاپها و تلفنهای هوشمند از این ساختار پیروی میکنند.
حال فرض کنیم که باتری شارژی لیتیومی در داخل یک پیچگوشتی شارژی قرار گرفته و میخواهیم کلید دستگاه را فشار بدهیم و از آن استفاده کنیم. با فشار دادن کلید دستگاه، انرژی الکتریکی موجود در باتری تخلیه میشود و تولید انرژی به وسیله انجام فرآیند اکسیداسیون در بخش آند و میان عنصر لیتیوم و ماده الکترولیت موجود در سلول باتری صورت میگیرد. در این حالت الکترونها از اتمهای لیتیوم جدا شده و باعث ایجاد یونهای لیتیوم میشوند.
الکترولیت و جداکننده، عامل ایجاد جریان الکترونی
علاوه بر آند و کاتد، الکترولیت و جداکننده نیز به عنوان دو جز بسیار مهم در انجام واکنش شیمیایی در باتریهای لیتیومی محسوب میشوند. الکترولیت، یک محلول پیچیده است که در باتریهای لیتیوم-یونی معمولا از یک محلول بر پایه اتر استفاده میشود. ساختار این محلول بگونهای است که مانع عبور الکترونها از حفرههای میکروسکوپی موجود در لایه جداکننده میشود اما یونهای لیتیوم را به راحتی از این بخش عبور میدهد.
یک یون به اتمی گفته میشود که با گرفتن یا از دست دادن الکترون، دارای بار خالص منفی یا مثبت میشود. همچنین الکترونها همیشه در مسیری حرکت میکنند که دارای کمترین میزان مقاومت الکتریکی باشد؛ بنابراین به دلیل ایجاد مقاومت توسط محلول الکترولیت، الکترونهای جدا شده از اتمهای لیتیوم از پایه آند خارج شده و با عبور از مدار بسته دستگاه، انرژی موردنیاز برای راهاندازی پیچگوشتی شارژی را فراهم میکنند و از طرف دیگر به بخش کاتد منتقل میشوند.
یونهای مثبت لیتیوم نیز تحت نیروی الکتریسیته ساکن و به کمک محلول الکترولیت از دیواره جداکننده به سمت کاتد حرکت کرده و در این بخش الکترونهای از دست داده خود را مجددا دریافت میکنند و طی یک فرآیند کاهشی به اتمهای لیتیوم تبدیل میشوند.
انجام فرآیند معکوس برای شارژ باتریهای لیتیومی
برای شارژ باتری لیتیومی باید فرآیند بالا را به شکل معکوس انجام بدهیم که این کار با اعمال یک جریان الکتریکی خارجی به وسیله شارژر انجام میشود. در واقع حضور جریان الکتریکی به انجام واکنش افزایشی در کاتد و انجام واکنش کاهشی در آند میانجامد. در این حالت الکترونها در جهت معکوس از اتمهای لیتیوم جدا شده و به پایه آند منتقل میشوند و یونهای مثبت لیتیوم نیز با عبور از بخش جداکننده در قسمت آند با الکترونها ترکیب شده و به این ترتیب فرآیند شارژ باتری انجام میشود.
باتریهای غیرقابل شارژ با نام سلولهای اولیه و باتریهای قابل شارژ با نام سلولهای ثانویه شناخته میشوند. در سلولهای اولیه، بخش کاتد همیشه به عنوان الکترود مثبت و بخش آند به عنوان الکترود منفی عمل میکند اما در سلولهای ثانویه امکان تغییر قطبیت الکترودها وجود دارد و به این ترتیب امکان شارژ سلولها فراهم میشود.
سلولهای ثانویه در زمان تخلیه هیچ تفاوتی با سلولهای اولیه ندارند اما در زمان شارژ، کاتد سلولهای ثانویه به الکترود منفی و آند آنها به الکترود مثبت تبدیل میشود.
باتری های لیتیومی چه کاربردی دارند و در کجاها استفاده میشوند؟
امروزه باتریهای لیتیومی برای تامین انرژی طیف وسیعی از تجهیزات سیار و قابل حمل مورد استفاده قرار میگیرند که از جمله آنها میتوان به موارد زیر اشاره کرد.
تجهیزات الکترونیکی قابل حمل: محصولاتی مانند تلفنهای هوشمند، لپتاپ، تبلت و سایر محصولاتی که علاوه بر ظرفیت شارژدهی بالا به کمترین میزان وزن و فضای اشغال شده توسط باتریها نیاز دارند.
وسایل نقلیه الکتریکی: باتری های لیتیومی به دلیل برخورداری از طول عمر بالا، پایداری عالی و سرعت شارژ بیشتر به شکل گسترده در صنعت خودروهای برقی مورد استفاده قرار میگیرند.
سیستمهای ذخیرهسازی انرژیهای تجدیدپذیر: انرژی الکتریکی تولیدشده توسط پنلهای خورشیدی و توربینهای بادی معمولا در داخل مجموعهای از باتری های لیتیومی ذخیره میشود تا در زمان اوج مصرف یا در زمان قطعی یا عدم تولید انرژی برق مورد استفاده قرار بگیرد.
قطعات پزشکی قابل حمل: استفاده از باتری های لیتیومی به شکل گسترده در تولید ضربانسازها، سمعکها و سایر دستگاههای پزشکی استفاده میشوند و با اشغال فضای بسیار کم، نرخ تخلیه ناچیز و طول عمر بالا نقش بسیار مهمی در عملکرد پایدار و طولانیمدت این محصولات دارند.
صنعت هوافضا: ظرفیت و پایداری بسیار زیاد باتری های لیتیومی، آنها را به یک انتخاب ایدهآل برای استفاده در فضاپیماها و ماهوارهها تبدیل کرده است.
صنایع نظامی و دفاعی: بسیاری از تجهیزات نظامی دقیق اعم از هواپیماهای بدون سرنشین، تجهیزات دید در شب و تجهیزات ارتباطی پرتابل برای ارائه عملکرد پایدار و بیصدا از باتری های لیتیومی برای تامین انرژی خود استفاده میکنند.
بدون شک رشد و توسعه باتری های لیتیومی ادامه خواهد داشت و حتی احتمال جایگزینی و استفاده از مواد و تکنولوژیهای جدید نیز در این حوزه وجود دارد اما موضوع غیرقابل انکار آن است که باتری های لیتیومی در حال حاضر وظیفه تامین انرژی بسیاری از ابزارها و تجهیزات روزمره انسانها را در اختیار دارند؛ موضوع بسیار مهمی که حتی فکر کردن به آن نیز تا چند دهه پیش امکانپذیر نبود.
مزایای باتری های لیتیومی در مقایسه با سایر تکنولوژیها
پایداری عالی و ارائه ظرفیت ذخیرهسازی بالا در ابعاد فیزیکی کوچک و وزن کم از مهمترین دلایل برتری باتری های لیتیومی در مقایسه با نمونههای دیگر هستند. تصور کنید که یک تلفن همراه با داشتن یک باتری اسیدی چه حجمی از فضای جیب شما را اشغال میکند یا سنگینی باتریهای بزرگ چه نتیجه معکوسی بر روی عملکرد خودروهای برقی خواهد داشت. البته باید در نظر داشت که دسترسی و تولید مواد باکیفیت مانند اکسید لیتیوم کبالت یا مواد دیگر به شکل مستقیم در کارآیی و کیفیت باتری های لیتیومی موثر خواهد بود.
از دیگر ویژگیهای مهم باتری های لیتیومی میتوان به ثابت ماندن ظرفیت حتی از پس از شارژ و تخلیههای مکرر، امکان شارژ با سرعت بیشتر و عدم تخلیه ناخواسته و حفظ انرژی برای مدتهای طولانی اشاره کرد.
آشنایی با انواع باتری های لیتیومی
همانطور که گفته شد، باتری های لیتیومی بر مبنای مواد مورد استفاده در ساختار داخلی آنها نامگذاری و دستهبندی میشوند که از مهمترین آنها میتوان به اکسید لیتیوم کبالت (LCO)، اکسید لیتیوم منگنز (LMO)، نیکل منگنز اکسید کبالت (NMC)، باتریهای لیتیوم پلیمری (LiPo) و لیتیوم آهن فسفات (LFP / LiFeP04) اشاره کرد.
در بین موارد فوق، نمونههای NMC به دلیل ظرفیت ذخیرهسازی و چگالی بالا، عمر طولانی و هزینه ساخت پایین از محبوبیت بسیار زیادی برخوردار هستند. نمونههای LFP نیز از جمله باتریهای با سطح ایمنی و طول عمر بالا محسوب میشوند اما در مقایسه با سایر نمونهها دارای چگالی انرژی یا ظرفیت ذخیرهسازی کمتری هستند.
نمونههای LCO نیز علیرغم ارائه ظرفیت ذخیرهسازی بسیار زیاد، به ندرت در خودروهای برقی و تجهیزات ذخیرهسازی مورد استفاده قرار میگیرند که از مهمترین دلایل این موضوع میتوان به محدودیتها و دشواریهای موجود در زمینه ساخت، نگهداری و استفاده از تجهیزات شارژ و تخلیه این قبیل از باتریها اشاره کرد.
در زمینه تولید خودروهای برقی معمولا از انواع دیگری از باتری های لیتیومی مانند اکسید لیتیوم تیتانیوم (LTO) یا اکسید آلومینیوم لیتیوم نیکل کبالت (NCA) استفاده میشود.
مشکلات و نقاط ضعف باتری های لیتیوم یونی
بدون شک باتری های لیتیوم یونی نیز دارای محدودیتها و نقاط ضعف مختلفی هستند. به عنوان مثال مواد به کار رفته در ساختار این باتریها در دسته عناصر کمیاب کره زمین قرار دارند که این موضوع باعث افزایش چشمگیر قیمت باتریهای لیتیوم یونی در مقایسه با نمونههای دیگر میشود. از طرفی باتری های لیتیوم یونی در برابر افزایش دما آسیبپذیر هستند. همچنین امکان تخلیه کامل سلولهای مورد استفاده در باتری های لیتیوم یونی بدون تخریب ساختار داخلی و استفاده از تجهیزات الکترونیکی خاص امکانپذیر نیست. و در نهایت اینکه افزایش بیرویه دما در باتریهای لیتیوم یونی باعث ایجاد آتشسوزی و از بین رفتن کامل آنها میشود.
دلیل وقوع انفجار گرمایی در باتری های لیتیوم یونی به این دلیل است که افزایش دما به تخریب لایه جداکننده منجر میشود و با ایجاد یک حالت اتصال کوتاه و تحریک ناگهانی یونها به ایجاد یک انفجار کوچک یا آتشسوزی میانجامد. به همین علت است که بسیاری از تولیدکنندگان از زمان اعلام خطرناک بودن باتری های لیتیوم یونی، از خردهفروشی سلولهای 18650 یا 2170 خودداری میکنند.
مقایسه باتری های لیتیوم یونی تک-سلول و چند-سلول
تا اینجا ما تنها در مورد یک سلول از باتری های لیتیوم یونی صحبت کردیم اما باید توجه داشته باشیم که بسیاری از باتریهای مورد استفاده در ابزارهای برقی از چند سلول تشکیل میشوند. به عبارت دیگر با سیمکشی و اتصال چندین سلول به یکدیگر میتوان آنها را به طور همزمان مورد استفاده قرار داد یا آنها را شارژ کرد. اتصال سلولها به یکدیگر باعث افزایش ظرفیت باتری و مدت زمان استفاده از ابزارهای مختلف میشود.
نحوه ساخت یک باتری چند-سلولی برای ابزارهای برقی
به طور خلاصه متوجه شدیم که باتریهای لیتیوم یونی دارای ساختار مشابه با نمونههای نیکل-کادمیم یا نیکل-فلز هستند اما هر ترکیب شیمیایی دارای خواص متفاوتی است و در حال حاضر باتری های لیتیوم یونی به عنوان بهترین نمونه در زمینه ذخیرهسازی و انتقال انرژی محسوب میشوند.
در حال حاضر تولیدکنندگان برای ساخت یک باتری چند-سلولی و تغذیه یک ابزار برقی از چندین سلول مجزا در حالت اتصال سری برای دستیابی به ولتاژهای بالاتر استفاده میکنند. مانند اتصال 3 سلولی برای دستیابی به ولتاژ 10.8 یا 12 ولت، اتصال 5 سلولی برای دستیابی به ولتاژ 18 یا 20 ولت، اتصال 6 سلولی برای دستیابی به ولتاژ 21.6 یا 24 ولت یا اتصال 10 سلولی برای دستیابی به ولتاژ 36 یا 40 ولت!
باتریهای با ولتاژ بالاتر مانند باتریهای 56، 58، 60 و 80 ولتی نیز وجود دارند که معمولا برای تغذیه تجهیزات برقی در فضاهای باز یا ابزارهای بسیار بزرگ استفاده میشوند. به طور کلی با اتصال سلولها در حالت سری میتوان به ولتاژهای بالاتر دست پیدا کرد.
ساخت باتری چند-سلولی با قدرت شارژدهی و ظرفیت بیشتر
با اتصال موازی باتریها، به عنوان مثال با اتصال موازی دو گروه 5تایی، میتوان به ظرفیتهای بالاتر دست پیدا کرد. افزایش ظرفیت باتری به این معناست که میتوان از یک دستگاه برای مدت زمان بیشتری استفاده کرد یا توان بیشتری از دستگاههای برقی به دست آورد. به عبارت دیگر با اتصال موازی سلولهای باتری، میزان Ah نهایی افزایش مییابد.
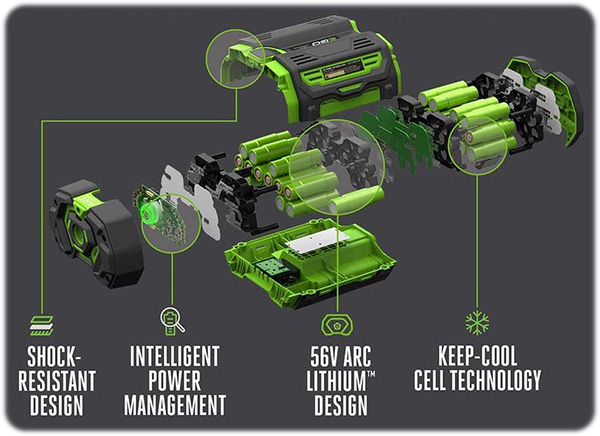
تولیدکنندگان با ترکیب سلولهای باتری در حالتهای سری و موازی به مقادیر دلخواه خود دست پیدا میکنند و مجموعه نهایی را در داخل یک محفظه یا پَک باتری قرار میدهند تا مشکلی از بابت دما، آلودگی یا رطوبت برای سلولها ایجاد نشود. همچنین مدارهای الکترونیکی پیشرفتهای نیز در ساخت باتریها بکار میروند تا از سلولهای باتری در زمان شارژ یا در حین استفاده از دستگاه، محافظت کنند. به این ترتیب یک باتری شارژی برای تغذیه ابزارهای برقی ساخته میشود.
در واقع میتوانیم بگوییم که باتریها شبیه به جعبههای جادویی کوچکی هستند که همیشه در کنار ما حضور دارند و زندگی امروز ما به شکل غیرقابل باوری به وجود آنها گره خورده است.